Ce document décrit la procédure opératoire standard (SOP) pour la reconstitution d'un flacon de rétatrutide lyophilisé à l'aide d'eau bactériostatique, dans un cadre de recherche in vitro. Il détaille le matériel, le protocole étape par étape, les calculs de concentration correspondant aux bras de dosage de l'essai analyse de l'essai NEJM, ainsi que les conditions de stockage post-reconstitution.
Cadre légal et préambule
Ce guide décrit une procédure de laboratoire pour la reconstitution d'un peptide de recherche destiné à la recherche scientifique in vitro et en laboratoire uniquement. Not for Human Use. Aucune partie de ce guide ne constitue une instruction pour un usage humain ou animal. Le rétatrutide est un peptide de recherche non approuvé par les autorités sanitaires (ANSM, EMA, FDA) pour quelque usage thérapeutique que ce soit.
1. Matériel nécessaire
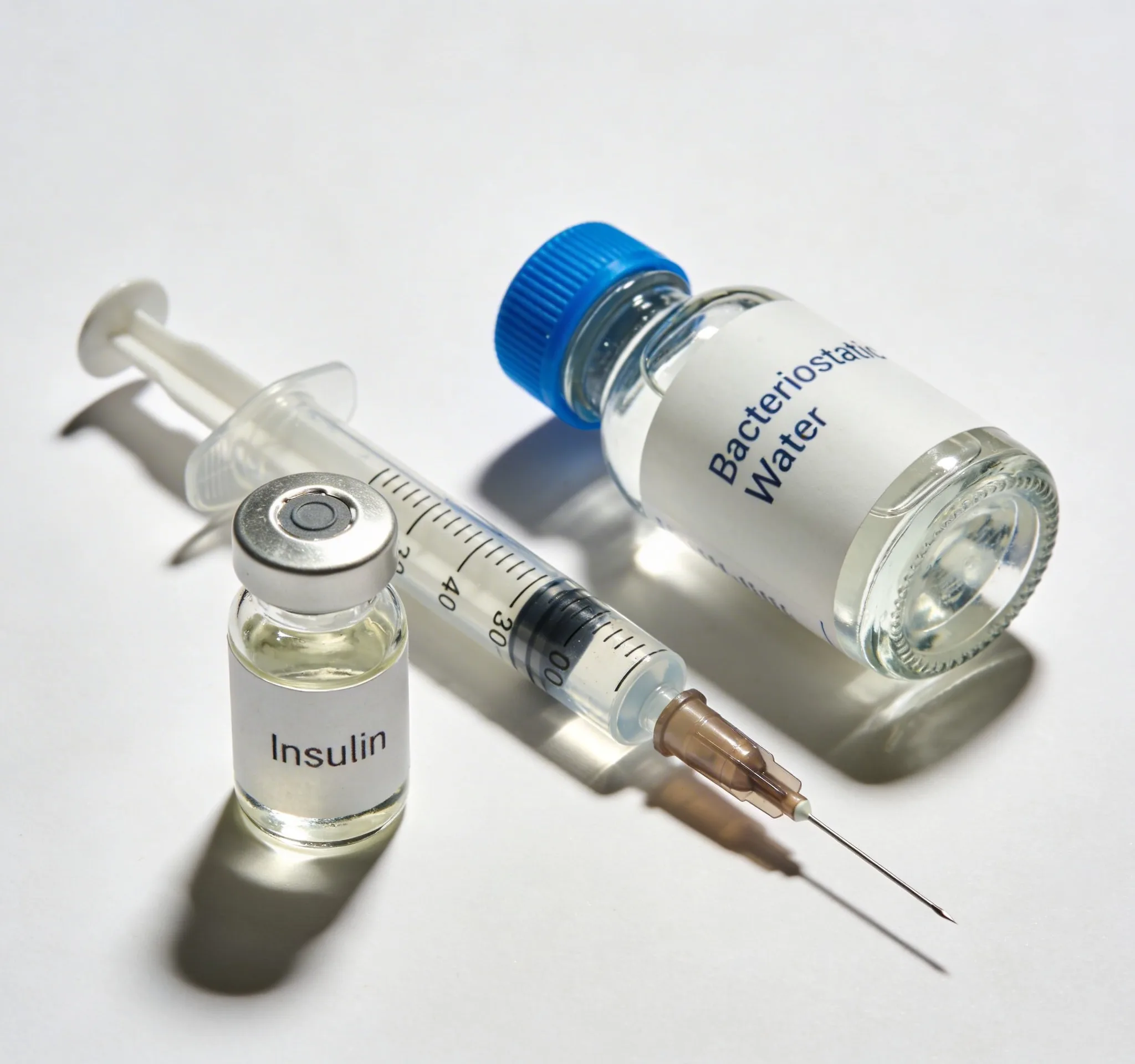
La procédure nécessite le matériel de laboratoire suivant, préalablement vérifié et stérile :
- Flacon de rétatrutide lyophilisé — dosage 10 mg, 20 mg ou 30 mg selon le lot de recherche
- Eau bactériostatique — solution aqueuse stérile contenant 0,9% d'alcool benzylique, grade USP, utilisée comme solvant standard pour la reconstitution des peptides de recherche
- Seringue stérile 1 mL (type insuline, graduation 100 UI) avec aiguille 29G ou 30G
- Tampons d'alcool isopropylique 70% pour désinfection des bouchons
- Gants nitrile non poudrés
- Zone de travail désinfectée, idéalement sous hotte à flux laminaire
- Étiquettes de traçabilité et journal de laboratoire pour documentation du lot
Le choix de l'eau bactériostatique plutôt que de l'eau pour préparation injectable (WFI) est standard dans les protocoles de recherche peptidique : l'alcool benzylique inhibe la prolifération bactérienne et permet l'usage multidose du flacon reconstitué sur plusieurs semaines de manipulation en laboratoire.
2. Préparation de l'environnement
La préparation de l'environnement de travail précède toute manipulation du matériel lyophilisé. Le flacon de rétatrutide et le flacon d'eau bactériostatique sont sortis du réfrigérateur et laissés à température ambiante pendant 15 à 20 minutes avant la procédure. Cette équilibration thermique réduit la formation de bulles lors du transfert et limite le choc thermique subi par la poudre lyophilisée.
La surface de travail est nettoyée à l'alcool isopropylique 70%. Les mains sont lavées selon le protocole standard, puis les gants nitrile sont enfilés. Tout matériel non nécessaire est retiré de la zone de manipulation afin de limiter les sources de contamination croisée.
3. Protocole de reconstitution étape par étape
La procédure ci-dessous est exécutée de manière continue, sans interruption entre les étapes, afin de limiter l'exposition à l'air ambiant.
- Désinfection du bouchon lyophilisé — Le bouchon en caoutchouc du flacon de rétatrutide est désinfecté par passage d'un tampon d'alcool isopropylique 70%. Laisser sécher 10 secondes.
- Désinfection du bouchon du solvant — Le bouchon du flacon d'eau bactériostatique est désinfecté de la même manière.
- Aspiration du solvant — Le volume d'eau bactériostatique cible est aspiré dans la seringue stérile (voir section 5 pour le choix du volume selon la concentration souhaitée).
- Insertion dans le flacon lyophilisé — L'aiguille est insérée dans le bouchon du flacon de rétatrutide. Le jet de solvant est dirigé contre la paroi interne du flacon, jamais directement sur la poudre lyophilisée.
- Transfert lent du solvant — Le solvant est injecté lentement. Le vide partiel présent dans le flacon facilite l'aspiration ; il n'est pas nécessaire de forcer le transfert.
- Retrait de la seringue — La seringue est retirée sans secousse. La seringue usagée est immédiatement jetée dans un conteneur DASRI.
- Homogénéisation par rotation — Le flacon est roulé doucement entre les paumes des mains pendant 30 à 60 secondes. Le flacon n'est jamais secoué : l'agitation mécanique dénature les liaisons tertiaires du peptide et génère une mousse qui complique le prélèvement ultérieur.
- Contrôle visuel — Après 1 à 2 minutes, la solution doit apparaître limpide, sans particules en suspension ni résidus solides. Toute opacité persistante ou présence de particules invalide la préparation.
4. Concentrations obtenues selon le volume de solvant
Le volume d'eau bactériostatique ajouté détermine la concentration finale de la solution reconstituée. Le tableau ci-dessous récapitule les combinaisons usuelles pour les dosages de flacons couramment rencontrés.
| Flacon lyophilisé | Volume de solvant | Concentration obtenue | Équivalence (UI / mg) |
|---|---|---|---|
| 10 mg | 1 mL | 10 mg/mL | 10 UI = 1 mg |
| 10 mg | 2 mL | 5 mg/mL | 20 UI = 1 mg |
| 10 mg | 3 mL | 3,33 mg/mL | 30 UI = 1 mg |
| 20 mg | 2 mL | 10 mg/mL | 10 UI = 1 mg |
| 30 mg | 3 mL | 10 mg/mL | 10 UI = 1 mg |
Les concentrations à 5 mg/mL et 10 mg/mL correspondent aux formulations utilisées dans les bras de dosage publiés dans l'essai NEJM 2023. La concentration à 5 mg/mL est la plus fréquemment retenue car elle permet un prélèvement en volume supérieur, réduisant l'erreur de graduation sur la seringue 1 mL.
5. Calcul du volume à prélever selon la dose NEJM
Les bras de dosage documentés dans le protocole de dosage NEJM 2023 sont 2 mg, 4 mg, 8 mg et 12 mg hebdomadaires. Le tableau ci-dessous indique le volume de prélèvement théorique correspondant, exprimé en UI sur une seringue à insuline 1 mL graduée au centième.
| Dose NEJM | À 10 mg/mL (volume) | À 10 mg/mL (UI) | À 5 mg/mL (volume) | À 5 mg/mL (UI) |
|---|---|---|---|---|
| 2 mg | 0,20 mL | 20 UI | 0,40 mL | 40 UI |
| 4 mg | 0,40 mL | 40 UI | 0,80 mL | 80 UI |
| 8 mg | 0,80 mL | 80 UI | 1,60 mL | 160 UI |
| 12 mg | 1,20 mL | 120 UI | 2,40 mL | 240 UI |
Ces volumes sont présentés à titre de référence documentaire pour la mise en correspondance des concentrations reconstituées avec les bras de dosage publiés. Ils ne constituent pas une posologie humaine. Le profil de tolérance observé dans l'essai est détaillé dans l'article profil de sécurité documenté.
6. Stockage après reconstitution
La solution reconstituée est conservée au réfrigérateur, entre 2°C et 8°C, à l'abri de la lumière directe. Le flacon est étiqueté avec la date de reconstitution, le volume de solvant ajouté et la concentration calculée, conformément aux exigences de traçabilité du laboratoire.
La stabilité documentée du rétatrutide en solution reconstituée à 2-8°C est d'environ 4 semaines. Au-delà de cette période, la dégradation du peptide devient non négligeable et le matériel doit être considéré comme inutilisable pour la recherche.
Avant reconstitution, le flacon lyophilisé est stable :
- À -20°C — stockage longue durée, stabilité supérieure à 24 mois
- À 2-8°C — stockage intermédiaire, stabilité 12 à 18 mois
- À 15-25°C (température ambiante) — stockage de transit jusqu'à 24 mois selon les certificats fournisseurs
La congélation d'une solution déjà reconstituée est déconseillée : les cycles de congélation/décongélation provoquent la formation de cristaux de glace qui fragmentent la structure tertiaire du peptide.
7. Erreurs fréquentes à éviter
Les erreurs ci-dessous sont documentées comme causes majeures de dégradation ou de contamination du matériel de recherche lors de la reconstitution :
- Jet de solvant dirigé sur la poudre — provoque une formation excessive de bulles et une dénaturation localisée du peptide. Le jet doit toujours être dirigé contre la paroi du flacon.
- Agitation par secousses — l'agitation mécanique rompt les liaisons tertiaires du peptide. Seule une rotation douce est utilisée pour l'homogénéisation.
- Stockage prolongé à température ambiante — la solution reconstituée hors réfrigération se dégrade rapidement et perd son intégrité en quelques jours.
- Utilisation d'eau du robinet, d'eau déminéralisée ou d'eau pour injection non bactériostatique — expose à un risque de contamination microbienne et invalide le matériel pour toute mesure quantitative.
- Cycles de congélation/décongélation répétés — la formation de cristaux de glace dégrade la structure du peptide.
- Réutilisation de seringue — source majeure de contamination croisée. Une seringue neuve et stérile est utilisée pour chaque prélèvement.
- Oubli de l'équilibration thermique — manipuler un flacon sortant directement du réfrigérateur augmente la condensation et favorise la formation de bulles.
8. Documentation recommandée pour le laboratoire
La traçabilité est une exigence centrale de tout protocole de recherche impliquant des peptides. Les éléments suivants sont consignés dans le journal de laboratoire à chaque opération de reconstitution :
- Étiquetage du flacon reconstitué — date de reconstitution, volume de solvant, concentration obtenue, numéro de lot du peptide et du solvant, initiales du manipulateur
- Journal de reconstitution — date, heure, opérateur, lot du rétatrutide, lot de l'eau bactériostatique, volume utilisé, observations (limpidité, bulles, anomalies)
- Traçabilité lot-date — conservation des certificats d'analyse (CoA) fournisseur associés au lot reconstitué, permettant le rapprochement ultérieur des résultats expérimentaux avec la matière première
- Suivi de stabilité — date d'ouverture du flacon reconstitué et date limite d'utilisation (J+28) notées en clair sur l'étiquette
Cette documentation permet la reproductibilité des manipulations et le rapprochement des données expérimentales avec la matière première utilisée. Pour la source du matériel de recherche, consulter acheter rétatrutide en France ou le comparatif prix des flacons de rétatrutide. Pour les étapes suivantes de manipulation en laboratoire, consultez notre guide technique d'injection du rétatrutide.
Disclaimer
Ce contenu est à vocation éducative pour chercheurs, techniciens de laboratoire et acheteurs de réactifs de recherche. Il ne constitue pas un conseil médical. Le rétatrutide est un peptide de recherche destiné exclusivement à la recherche scientifique in vitro et en laboratoire. Not for Human Use. Aucune partie de ce guide ne décrit ou ne recommande un usage humain ou animal.
Peptides de recherche : Pour une sélection complète de peptides de recherche avec documentation qualité (CoA, HPLC), consultez également acheter-peptides.fr — gamme complète.